
Thomas Dalton
0
1568
345
Oamenii de știință pot înțelege în sfârșit tranziția misterioasă din spatele unui experiment de chimie vechi de un secol. Detaliile acestei transformări, în care adăugarea de electroni la o soluție de amoniac albastru strălucitor o transformă într-un bronz lustros, metalic, au evitat de mult timp oamenii de știință.
Noul studiu dezvăluie detaliile subtile ale acestei schimbări și arată că această transformare este treptată, mai degrabă decât bruscă. „Ceea ce am făcut cu succes este că am înțeles destul de mult cum se comportă aceste soluții la o gamă largă de concentrații folosind o tehnică microjet”, a declarat co-autorul studiului Ryan McMullen, un doctorat în chimie la Universitatea din sudul Californiei . Această tehnică, care implică fotografierea fluxurilor subțiri ale soluției printr-un vid, nu a mai fost utilizată pe lichidul lucios înainte.
Iar descoperirea ar putea deschide noi tipuri de reacții în chimia organică în viitor, a spus McMullen .
Legate de: 8 elemente chimice despre care nu ați auzit niciodată
Ce este un metal?
Metalele sunt un grup divers. Unele, cum ar fi litiu, sunt suficient de ușoare pentru a pluti, în timp ce altele, precum plumbul sau osmiul sunt extrem de dense. Unele necesită temperaturi incredibil de ridicate pentru a se topi, în timp ce altele se topește ușor (Mercur, de exemplu, se topește la minus 38,3 grade Celsius sau minus 37,9 grade Fahrenheit). În cele din urmă, ceea ce metalele au în comun este capacitatea lor de a conduce electricitate la zero absolut, punctul în care mișcarea moleculară din căldură se oprește în esență..
Dar cum se transformă unele nemetale în metale? Într-un nou studiu, cercetătorii au răspuns la această întrebare adăugând metale în amoniac lichid.
În primul rând, cercetătorii au condensat amoniacul, care este un gaz la temperatura camerei, într-un lichid răcindu-l până la 27,4 F negativ (minus 33 C). Au adăugat apoi sodiu, litiu sau potasiu, care sunt toate metalele alcaline. (Mai degrabă faimos, aceste metale reacționează exploziv atunci când sunt scufundate în apă.) Experimentele au fost realizate în colaborare cu oameni de știință de la Academia Cehă de Științe și Institutul Fritz-Haber al Societății Max Planck din Berlin, precum și cercetători din Japonia și Franța.
Legate de: Top 10 cele mai mari explozii din toate timpurile
Rezultatul a fost o reacție așteptată: Amoniacul lichid a scos electroni din metal. Acei electroni au devenit apoi prinși între moleculele de amoniac, creând așa-numiții electroni solvați pe care cercetătorii sperau să le studieze. La concentrații scăzute, rezultatul a fost un lichid albastru, nemetalic. Pe măsură ce electronii solvați sau prinși, soluția a trecut la bronz strălucitor.
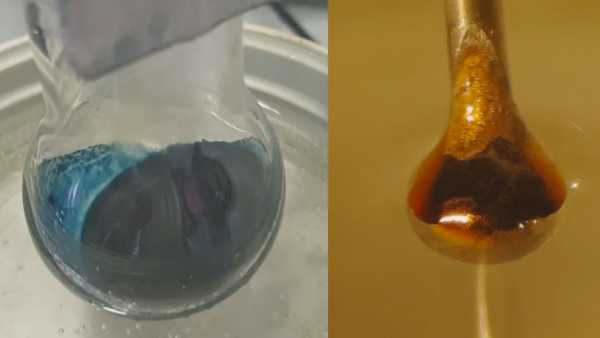
Următoarea provocare a fost investigarea modului în care electronii solvați s-au comportat la diferite concentrații. Aceasta a implicat împușcarea unui microjet al soluției - aproximativ lățimea unui păr uman - printr-un fascicul de raze X sincrotron, care sunt fascicule cu raze X cu energie mare. Razele X au excitat electronii solvați, determinându-i să scape din colivia lichidă a moleculelor de amoniac. Cercetătorii au putut apoi să măsoare câtă energie a fost nevoie pentru a elibera electronii solvați.
Cercetătorii au descoperit că, cu cât concentrația electronilor solvați este mai mare, cu atât modelul de eliberare de energie se potrivește cu ceea ce se vede într-un metal. Iată ce înseamnă asta: Dacă grafică cantitatea de energie necesară pentru eliberarea electronilor din cușca lor cu amoniac lichid, metalele au în mod obișnuit ceea ce se numește „muchie Fermi”, o tranziție foarte bruscă, a spus McMullen. La concentrații mai mici de electroni solvați, acest grafic cu eliberare de energie arată mai mult ca o colină rotunjită. Numai la concentrații mai mari de electroni a apărut această margine Fermi. Marginea reflectă cât de mult au electronii de energie la o temperatură dată, a adăugat McMullen.
"Când crești concentrația la gama metalică, atunci vezi, acest model minunat apare foarte, foarte caracteristic pentru un metal", a spus McMullen.
Rezultatele au fost interesante deoarece au arătat că lichidul asemănător metalului creat prin combinarea metalelor alcaline și a amoniacului este de fapt un metal la nivel fizic fundamental, a spus el.
"Este un metal autentic, nu este ceva care arată doar ca unul", a spus McMullen.
Electronii solvați cu concentrație mai mică sunt folosiți într-un tip de reacție numit reacție de mesteacăn, care adaugă electroni structurilor moleculare numite inele aromatice. Acest tip de reacție a fost utilizat la fabricarea primelor pilule contraceptive orale în anii '50, a spus McMullen. Înțelegând cum funcționează electronii solvați la concentrații mari, cercetătorii pot găsi potențial noi tipuri de reacții chimice, a spus el. De exemplu, ei ar putea excita electronii solvați cu fascicule de lumină pentru a-i determina să se comporte în moduri noi.
„Dacă bifați puțin electronii astfel încât să fie mai excitați din punct de vedere energetic, puteți începe să priviți câteva reacții nebune care nu s-ar întâmpla altfel niciodată”, a spus McMullen.
Cercetătorii au raportat concluziile lor pe 5 iunie în revista Science.
Vezi toate comentariile (2)














